-
Use Cases
-
Resources
-
Pricing
Modelo Atómico
Events
Modelo Atómico de Demócrito
5000 A.C.
% complete
Demócrito fue el filósofo griego que postuló por primera vez un modelo acerca del átomo. Desarrolló la “Teoría Atómica del Universo” la cual, no se apoyaba de experimentos, sino de razonamientos lógicos. Demócrito decía que la materia es una mezcla de elementos que poseen las mismas características, comprendidos de entidades infinitamente pequeñas, que no podríamos observar a simple vista, llamándolos átomos.
Principios fundamentales del Modelo atómico de Demócrito.
Estos átomos son físicamente indivisibles.
Entre cada átomo hay un espacio vacío.
Los átomos son indestructibles.
Los átomos están continuamente en movimiento.
Hay muchos tipos de átomos.

Modelo Atómico de Dalton
1803
% complete
Con base en los resultados de sus investigaciones, Dalton pudo demostrar que los átomos realmente existen, algo que Demócrito solo había inferido, creando una de las teorías más importantes en la historia de la física moderna.
Gracias a este modelo se considera al átomo como la partícula fundamental de la materia, con la característica de que al agruparse forman moléculas.
Los puntos más importantes de su teoría son:
1)Los elementos están formados por átomos
2)Los átomos de un mismo elemento son todos iguales entre sí.
3)Los compuestos se forman por la unión de átomos de distintos elementos, combinados de manera sencilla y constante formando entidades bien definidas llamadas moléculas.

Modelo Atómico de Thomson
1897
% complete
Thompson presentó algunas hipótesis, tratando de justificar dos hechos:
1)La materia es eléctricamente neutra por lo que, además de contener electrones, debe de haber partículas con cargas positivas.
2)Los electrones pueden extraerse de los átomos, pero no las cargas positivas.
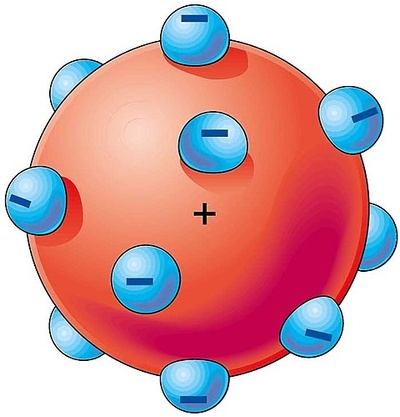
Su modelo consistía en una especie de “pastel” en la que los electrones aparecían incrustados como si fueran “trocitos de fruta”. De esta forma, pretendía explicar que la mayoría de la masa estaba asociada con la carga positiva y que había un número determinado de electrones distribuidos uniformemente dentro de esa masa con carga positiva.
Modelo Atómico de Lewis
1902
% complete
En 1916 Gilbert Newton Lewis propuso que el enlace covalente entre átomos se produce por compartición de pares de electrones, mecanismo por el que cada uno individualmente podría alcanzar ocho electrones en su capa más externa.
El fundamento de este principio hay que buscarlo en la denominada regla del octeto, consecuencia del desarrollo del modelo de Bohr y del descubrimiento de los gases nobles, sustancias de notable inercia química y ocho electrones en su capa de valencia. Para alcanzar el octeto electrónico los átomos pueden compartir más de un par de electrones (enlace simple), dando lugar a enlaces múltiples.
Se denomina orden o multiplicidad de enlace al número de pares de electrones compartidos.
Es uno de los primeros modelos atómicos descritos, y fue desarrollado para explicar el fenómeno de los electrones de valencia.
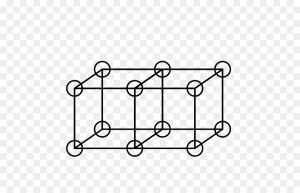
En este modelo atómico, los electrones de valencia se encuentran ubicados en los vértices de un hipotético cubo, que representa el átomo en cuestión.
Según Lewis, los átomos pueden obtener configuración electrónica estable por compartición de electrones. un átomo obtiene configuración estable de gas noble cuando posee en su última capa 8 electrones.
Los electrones no se transfieren de un átomo a otro, sino que se comparten al formar una molécula. Cada par de electrones compartidos constituye un enlace covalente.
El modelo de Lewis fue un paso importante en la historia de la Química para entender el significado del átomo pero se abandonó pronto esta teoría.
Gracias a esta teoría se conoció el concepto de "valencia de un electrón que en el último nivel de energía pueden reaccionar a
Modelo Atómico de Rutherford
1908
% complete
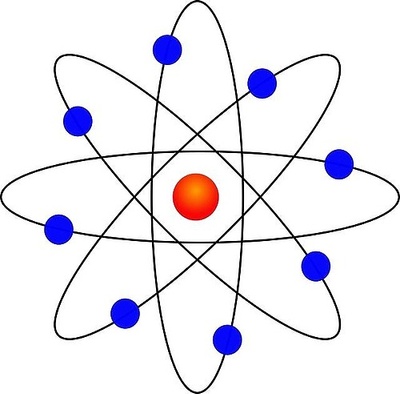
Identificó dos tipos de radiaciones a las que llamó alfa (α) y beta (β). Gracias a su experiencia en radiación, estableció un modelo molecular, que tiene las siguientes características:
1)El átomo tiene un núcleo central en el que está concentrada la carga positiva, y casi toda su masa.
2)En la zona exterior (corteza) se encuentra la carga negativa que está formada por electrones.
3)El núcleo contiene protones.
4)Los electrones giran alrededor del núcleo y están separados de éste por una gran distancia.
5)El tamaño del núcleo es muy pequeño en comparación con la del átomo.
Modelo Atómico de Bohr
1913
% complete
Bohr realizó estudios con hidrógeno y gracias a esto estableció que:
1)Los átomos que tienen el mismo número de electrones de valencia y que poseen distintos números, tienen características similares.
2)Los átomos tienen un núcleo demasiado pequeño y denso que contiene partículas subatómicas.
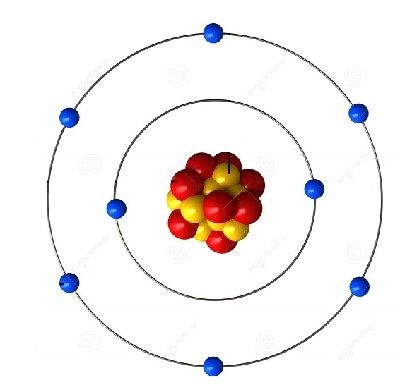
3)Los electrones se encuentran en diferentes órbitas alrededor del núcleo.
4)Los átomos son eléctricamente neutros, pero si tienen electrones cargados negativamente, deben contener otras partículas con carga positiva (protones).
En el modelo de Bohr, se estipula que la energía del electrón es mayor cuanto mayor sea el radio r.
Por lo cual, cuando el electrón salta a una órbita de menor radio, se pierde energía. Esa energía perdida es la que el átomo emite hacia el exterior en forma de un quanto de luz. Dicho de otro modo, en forma de fotón.
Modelo Atómico de Sommerfeld
1916
% complete
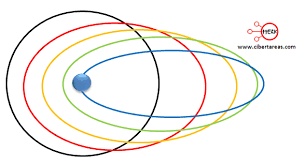
El modelo atómico de Sommerfeld, es una adaptación mejorada y generalizada del modelo atómico de Bohr, dándole a éste, un punto de vista relativista, pero aun así, no pudo explicar los modos de emisión que tenían las órbitas elípticas, pudiendo sólo descartar las órbitas circulares.
El modelo atómico de Sommerfeld surge para perfeccionar las deficiencias del modelo atómico de Bohr. Las proposiciones de este modelo, a grandes rasgos, son las siguientes:
– Los electrones describen órbitas circulares alrededor del núcleo, sin irradiar energía.
– No todas las órbitas eran posibles. Solo están habilitadas las órbitas cuyo momento angular del electrón cumpla con ciertas características. Vale acotar que el momento angular de una partícula depende de un compendio de todas sus magnitudes (velocidad, masa y distancia) con respecto al centro del giro.
– La energía liberada cuando un electrón desciende de una órbita a otra es emitida en forma de energía luminosa (fotón).
– Según las leyes electromagnéticas de Maxwell, todas las cargas sometidas bajo cierta aceleración emiten energía en forma de radiación electromagnética.
– Ante la postura de la física clásica, resultaba inconcebible que un electrón no pudiese orbitar libremente a cualquier distancia del núcleo.
– Para entonces, la comunidad científica tenía una firme convicción sobre la naturaleza ondulatoria de la luz, y la idea de que se presente como partícula no estaba contemplada hasta entonces.
Arnold Sommerfeld concluyó que la diferencia de energía entre los electrones —a pesar de que estos estuviesen en un mismo nivel energético— se debía a la existencia de subniveles energéticos dentro de cada nivel.
Modelo Atómico de Schrödinger
1926
% complete
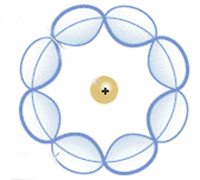
Schrödinger sugirió que el movimiento de los electrones en el átomo correspondía a la dualidad onda-partícula, y en consecuencia, los electrones podían movilizarse alrededor del núcleo como ondas estacionarias.
Características del modelo atómico de Schrödinger
-Describe el movimiento de los electrones como ondas estacionarias.
-Los electrones se mueven constantemente, es decir, no tienen una posición fija o definida dentro del átomo.
-Este modelo no predice la ubicación del electrón, ni describe la ruta que realiza dentro del átomo. Sólo establece una zona de probabilidad para ubicar al electrón.
-Estas áreas de probabilidad se denominan orbitales atómicos. Los orbitales describen un movimiento de traslación alrededor del núcleo del átomo.
-Estos orbitales atómicos tienen diferentes niveles y sub-niveles de energía, y pueden definirse entre nubes de electrones.
-El modelo no contempla la estabilidad del núcleo, sólo se remite a explicar la mecánica cuántica asociada al movimiento de los electrones dentro del átomo.
Modelo Atómico de Chadwick
1932
% complete
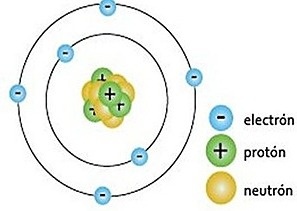
El modelo atómico de Chadwick se centra en la modelación del núcleo atómico constituido no solo por protones (cargas positivas), sino también por neutrones (cargas neutras).
El ahínco de Chadwick en demostrar la existencia de partículas neutras se generó en los años 20. Sin embargo, en esa época el destacado científico realizó múltiples intentos en vano.
Chadwick pensaba que la emisión de rayos gamma contenía partículas neutras, y que estas partículas eran las que habían chocado contra la muestra de cera, induciendo posteriormente la liberación de los protones de la cera.
Chadwick detectó que el comportamiento de los protones liberados por la cera solo podía explicarse si esas partículas hubiesen chocado contra otras partículas eléctricamente neutras, y con una masa muy parecida.
Dos semanas más tarde, James Chadwick publicó un artículo en la revista científica Nature sobre la posible existencia de neutrones.
Sin embargo, Chadwick concibió el modelo inicialmente considerando que el neutrón era un arreglo constituido por un protón y un electrón, lo cual generaba la carga neutra. Más adelante, el físico alemán Werner Heisenberg demostró que el neutrón era una partícula única y elemental.
REFERENCIAS
EQUIPO
Pineda Reyes Rocío Sheryl
Sánchez Hernández Camila Victoria