-
Use Cases
-
Resources
-
Pricing
El modelo atómico
Events
Democrito
460 a.C
% complete
Demócrito, 460-370 a. C., era un filósofo quien sostuvo que el mundo estaba formado por espacio vacío y pequeñas partículas llamadas átomos. Pensaba que los átomos son las partículas más pequeñas de la materia y que existen diferentes tipos de átomos según cada tipo de materia. La idea de que la materia está formada por partículas fundamentales llamadas átomos se conoce como teoría atómica de la materia.

Antoine Lavoisier
1782 - 1794
% complete
Lavoisier concluyó que, cuando se lleva a cabo una
reacción química, la materia no se crea ni se destruye: sólo se transforma. La conclusión de Lavoisier se conoce como ley de la conservación de la materia. Éste es otro nombre para la ley de la conservación de la masa

Proust
1799
% complete
Proust observó que la masa de los elementos que los forman siempre están en proporción. En la actualidad, este principio se conoce como ley de las proporciones definidas,

Teoría atómica de Dalton
1803 - 1807
% complete
Dalton consideró que una teoría atómica de la materia podría explicar las pruebas experimentales. Por ejemplo, si la materia estaba formada por átomos indivisibles, entonces una reacción química sólo re acomodaría esos átomos y no habría ni formación ni desaparición de ellos. Esta idea explicaría la ley de la conservación de la masa. También, si cada elemento constaba de átomos de un tipo y masa específicos, entonces un compuesto siempre presentaría cierta proporción de átomos que nunca variaba. Así, la teoría atómica de Dalton explicaba también la ley de las proporciones definidas.
Los siguientes postulados son los puntos
principales de la teoría atómica de Dalton:
- Toda la materia está compuesta por átomos.
- Los átomos son indestructibles y no pueden dividirse en partículas más pequeñas. (Es decir, los átomos son indivisibles.)
- Todos los átomos de un elemento son exactamente iguales entre sí, pero diferentes a los átomos de otros elementos.

Experimento de Thomson
1897
% complete
En 1897, un físico británico, J.J. Thomson, descubrió que el modelo de la esfera sólida no era correcto.
Thomson usó, en sus experimentos, un tubo al vacío, del cual se extrajeron todos los gases que contenía. En cada extremo del tubo se colocó una pieza metálica llamada electrodo conectada a una terminal metálica fuera del tubo. Estos electrodos adquieren una carga eléctrica cuando se conectan a una fuente de alto voltaje. Cuando los electrodos están cargados, unos rayos viajan en el tubo desde el electrodo negativo, que es el cátodo, hacia el electrodo positivo, que se llama ánodo. Debido a que el origen de estos rayos es el cátodo, se denominan rayos catódicos. Thomson descubrió que los rayos se desvían hacia una placa con carga positiva y se alejan de una placa con carga negativa. Él sabía que los objetos con cargas iguales se repelen entre sí, mientras que los objetos con cargas contrarias se atraen. Thomson concluyó que los rayos catódicos estaban constituidos por partículas invisibles con carga negativa, a las que llamó electrones. Los electrones provenían de la materia (átomos) del electrodo negativo.

Modelo atómico de Thomson
1904
% complete
En el modelo, el átomo está compuesto por electrones de carga negativa en un átomo positivo, incrustados en este al igual que las pasas de un pudin (o budín). Por esta comparación, fue que el supuesto se denomina Modelo del pudin de pasas Postulaba que los electrones se distribuían uniformemente en el interior del átomo, suspendidos en una nube de carga positiva. El átomo se consideraba como una esfera con carga positiva con electrones repartidos como pequeños gránulos

Experimento de Rutherford
1909
% complete
En 1909, un científico del equipo de Ernest Rutherford, en Inglaterra, llevó a cabo el primero de una serie de experimentos importantes que revelaron un ordenamiento muy diferente al modelo del pastel atómico.
El experimento consta de una cámara de protección de plomo que contiene polonio radiactivo, que emite un rayo de partículas subatómicas con carga positiva a través de un orificio. Actualmente sabemos que las partículas del rayo son agregados que contienen dos protones y dos neutrones llamados partículas alfa. Además, se había colocado una hoja de oro rodeada por una pantalla cubierta con sulfuro de zinc, que brillaba cuando era golpeada por las partículas con carga positiva del rayo.
El oro es un metal con el que se puede hacer una hoja de unos cuantos átomos de espesor.
El grupo de Rutherford utilizó
esta propiedad para realizar su experimento. Si el modelo planetario fuera válido, Rutherford y su equipo hubieran esperado ver que las
partículas alfa atravesaban la hoja.

modelo nuclear del átomo
1909
% complete
Para explicar los resultados del experimento, el equipo de Rutherford propuso un nuevo modelo para el átomo. Debido a que la mayoría de las partículas atravesaban la hoja concluyeron que el átomo era casi totalmente espacio vacío. Como algunas partículas se desviaban, propusieron que el átomo tenía una parte central pequeña, densa, con carga positiva,llamada núcleo.
Recuerda que el haz de partículas tiene carga positiva.
Si el núcleo tuviera carga negativa, estas partículas se
atraerían entre sí. Sin embargo, en el experimento de
Rutherford, algunas de las partículas alfa se desviaban.
Esto indicó que el núcleo es pequeño, denso y tiene
carga positiva.

Modelo atómico de Bohr
1913
% complete
En 1913, el físico danés Niels Bohr sugirió que los electrones giran alrededor del núcleo, igual que los planetas giran alrededor del sol. El modelo de Bohr estaba de acuerdo con el espectro de emisión producido por el átomo de hidrógeno, pero no podía extenderse a átomos más complejos. Las ideas básicas de la teoría de Bohr fueron que los electrones se mueven alrededor del núcleo del átomo, en trayectorias circulares, llamadas órbitas. Estas órbitas están a distancias definidas del núcleo y representan niveles energéticos que determinan la energía de los electrones.Los electrones de la órbita más cercana al núcleo tienen la menor energía; los más alejados del núcleo tienen mayor energía.
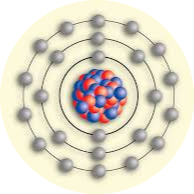
modelo atómico actual
1920
% complete
En el modelo atómico actual, los neutrones y protones forman un núcleo en el centro del átomo. Los electrones, con carga negativa, están distribuidos en el espacio alrededor del núcleo. Los electrones con mayor energía están más alejados del núcleo y ocupan el nivel energético externo. la evidencia de
la existencia de niveles energéticos surge de la interpretación de los espectros de emisión de los átomos. Es importante conocer sobre los niveles energéticos de los átomos, porque ayuda a explicar cómo éstos se enlazan entre sí y por qué forman una clase de compuestos, por ejemplo, iónicos o covalentes.
