-
Use Cases
-
Resources
-
Pricing
Renovación de la física atómica
Events
Antecedentes
1803
% complete
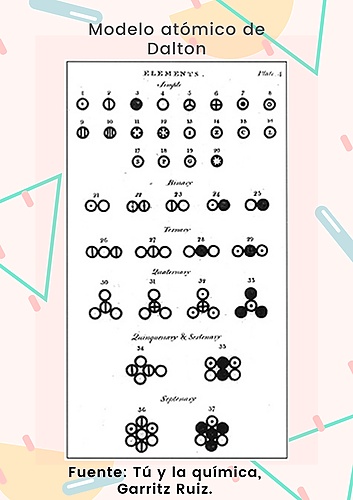
Mucho antes del siglo XX ya se hablaba del "átomo" y se descubren distintos elementos, pero es Dalton (1766-1844) un científico inglés quien introduce las ideas atómicas en la química y establece que la materia está compuesta de átomos de diferentes pesos. Establece su modelo atómico el cual dice que "los átomos tienen una forma de esfera solida".
Joseph John Thomson
1856 - 1940
% complete
Thomson nació el 18 de diciembre de 1856 en Cheetham Hill, un distrito de Mánchester en Inglaterra, y tenía ascendencia escocesa. En 1870 estudió ingeniería en el Owens College, hoy parte de la Universidad de Mánchester, y se trasladó al Trinity College de Cambridge en 1876. En 1880, obtuvo su licenciatura en Matemáticas (Segunda Wrangler y segundo premio Smith) y Maestría en Artes (obteniendo el Premio Adams) en 1883. En 1884 se convirtió en profesor de Física en Cavendish. Uno de sus alumnos fue Ernest Rutherford, quien más tarde sería su sucesor en el puesto. Thomson fue elegido miembro de la Royal Society el 12 de junio de 1884, y posteriormente fue su presidente de 1915 a 1920. En 1897 descubrió el electrón y propuso un modelo en el cual los electrones tenían cargas negativas al dentro de el átomo quien tenía carga positiva.
En 1890 se casó con Rose Elizabeth Paget, hija de sir Edward George Paget, médico, entonces Regius Profesor de Medicina (Regius Professor of Physic) en Cambridge. Con ella, fue padre de un hijo, George Paget Thomson, y una hija, Joan Paget Thomson. Su hijo se convirtió en un destacado físico, quien a su vez fue galardonado con el Premio Nobel de Física en 1937 por demostrar las propiedades de tipo ondulatorio de los electrones.
J. J. Thomson fue galardonado con el Premio Nobel de Física en 1906, «en reconocimiento de los grandes méritos de sus investigaciones teóricas y experimentales en la conducción de la electricidad generada por los gases». Fue nombrado caballero en 1908 y nombrado en la Orden del Mérito en 1912. En 1914 dio el Romanes Lecture en Oxford sobre la teoría atómica. En 1918 fue nombrado rector del Trinity College de Cambridge, donde conoció a Niels Bohr, donde permaneció hasta su muerte. Murió el 30 de agosto de 1940 y fue sepultado en la Abadía de Westminster, cerca de sir Isaac Newton.
Fuente: Cooks, R. G.; A. L. Rockwood , 'The 'Thomson'.

Ernest Rutherford
1871 - 1937
% complete
Ernest Rutherford, conocido también como Lord Rutherford (Reino Unido, 30 de agosto de 1871-Cambridge, 19 de octubre de 1937), fue un físico y químico británico nacido en Nueva Zelanda.
Se dedicó al estudio de las partículas radiactivas y logró clasificarlas en alfa (α), beta (β) y gamma (γ). Halló que la radiactividad iba acompañada por una desintegración de los elementos, lo que le valió para ganar el Premio Nobel de Química en 1908. Se le debe un modelo atómico, con el que probó la existencia del núcleo atómico, en el que se reúne toda la carga positiva y casi toda la masa del átomo. Consiguió la primera transmutación artificial con la colaboración de su discípulo Frederick Soddy.
Durante la primera parte de su vida se consagró por completo a las investigaciones, pasó la segunda mitad dedicado a la docencia y dirigiendo los Laboratorios Cavendish de Cambridge, en donde se descubrió el neutrón. Fue maestro de Niels Bohr y Otto Hahn.
Fuente: Gamov, George. Biografía de la física.

Niels Bohr
1885 - 1962
% complete
Nació en Copenhague, hijo de Christian Bohr, un devoto luterano y catedrático de fisiología en la universidad de la ciudad, y Ellen Adler, miembro de una adinerada familia judía de gran importancia en la banca danesa y en los «círculos del Parlamento». Tras doctorarse en la Universidad de Copenhague en 1911, e intentar la ampliación de estudios en el Cavendish Laboratory de Cambridge con el químico Joseph John Thomson, descubridor del electrón (el tema de la tesis doctoral de Bohr) y ganador del premio Nobel en 1922, quien no mostró un gran interés en el joven Bohr, completó sus estudios en Mánchester, teniendo como maestro a Ernest Rutherford, con el que estableció una duradera relación científica y amistosa.
En 1916, Niels Bohr comenzó a ejercer como profesor de física teórica en la Universidad de Copenhague, consiguiendo los fondos para crear el Instituto Nórdico de Física Teórica, que dirigió desde 1920 hasta su fallecimiento.
En 1943, con la Segunda Guerra Mundial en pleno apogeo, Bohr escapó a Suecia para evitar su arresto por parte de la policía alemana, viajando posteriormente a Londres. Una vez a salvo, apoyó los intentos angloamericanos para desarrollar armas atómicas, en la creencia de que la bomba alemana era inminente, y trabajó para ello en el Proyecto Manhattan de Los Álamos, Nuevo México (EE. UU.).
Después de la guerra, abogando por los usos pacíficos de la energía nuclear, retornó a Copenhague, ciudad en la que residió hasta su fallecimiento en 1962.
Fuente: Bronowski, J, El ascenso del hombre.

Renovación de la Física atómica
1895 - 2019
% complete

Modelo atómico de Thomson
1897
% complete
Thomson después de descubrir el electrón, describió su propio modelo atómico, En el modelo, el átomo está compuesto por electrones de carga negativa en un átomo positivo, incrustados en este al igual que las pasas de un pudín. Por esta comparación, fue que el supuesto se denominó «Modelo del pudín de pasas». Postulaba que los electrones se distribuían uniformemente en el interior del átomo, suspendidos en una nube de carga positiva. El átomo se consideraba como una esfera con carga positiva con electrones repartidos como pequeños gránulos. Pese a sus deficiencias y su breve vida, el modelo del “Pudín con pasas”
representó un paso importante en el desarrollo de la teoría atómica ya que incorporó partículas subatómicas y nuevos descubrimientos, como la existencia del electrón, e introdujo la noción del átomo como una masa no inerte y divisible. A partir de este modelo, los científicos supusieron que los átomos estaban compuestos de unidades más pequeñas, y que los átomos interactuaban entre sí a través de muchas fuerzas diferentes.

Modelo atómico de Rutherford
1911
% complete
Las partículas con carga positiva se encuentran en un volumen muy pequeño comparado con el tamaño del átomo. La mayor parte de la masa del átomo se encuentra en ese pequeño volumen central. Rutherford no lo llamó “núcleo” en sus papales iniciales pero lo hizo a partir de 1912. Los electrones con carga eléctrica negativa, giran alrededor del núcleo.
Los electrones gira a altas velocidades alrededor del núcleo y en trayectorias circulares a las que llamó órbitas. Tanto los electrones cargados negativamente como el núcleo con carga positiva
se mantienen unidos por una fuerza de atracción electrostática.

Modelo atómico de Bohr
1913
% complete
En 1913 Niels Bohr, desarrolló su célebre modelo atómico de acuerdo a cuatro postulados fundamentales:
Los electrones orbitan el átomo en niveles discretos y cuantizados de energía, es decir, no todas las órbitas están permitidas, tan sólo un número finito de éstas.
Los electrones saltan de un nivel energético a otro sin pasar por estados intermedios.
El salto de un electrón desde un nivel energético menor, a otro de mayor energía, implica la absorción de energía por parte del electrón, en el caso contrario, el electrón habrá emitido energía en forma de un único cuanto de luz (fotón) cuya energía corresponde a la diferencia de energía entre ambas órbitas.
Las órbitas permitidas tienen valores discretos del momento angular orbital L de acuerdo con la siguiente ecuación:
L=c* ħ=n(h/2π)x
Donde electrón = 1,2,3,… es el número cuántico angular o número cuántico principal.
La cuarta hipótesis asume que el valor mínimo de electrón es 1. Este valor corresponde a un mínimo radio de la órbita del electrón de 0.0529 nm. A esta distancia se le denomina radio de los . Un electrón en este nivel fundamental no puede descender a niveles inferiores emitiendo energía.
Se puede demostrar que este conjunto de hipótesis corresponde a la situación en la que los electrones estables orbitando un átomo están descritos por funciones de onda estacionarias. Un modelo atómico es una representación que describe las partes que tiene un átomo y como están dispuestas para formar un todo.
Basándose en la constante de Planck (E=hv) consiguió cuantizar las órbitas observando las líneas del espectro. el modelo atómico propuesto por Bohr, solo es válido para el átomo de hidrógeno o aquellos átomos que tienen un solo electrón.

Modelo atómico de Sommerfield
1916
% complete
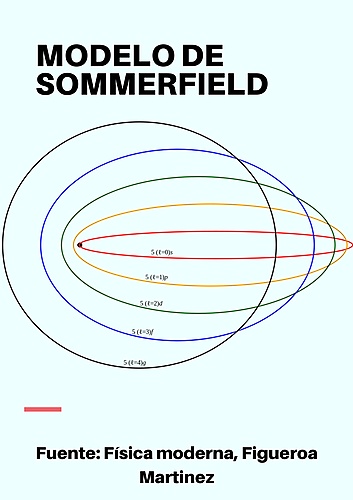
En 1916, Sommerfeld perfeccionó el modelo atómico de Bohr intentando paliar los dos principales defectos de este. Para eso introdujo dos modificaciones básicas: Órbitas casi-elípticas para los electrones y velocidades relativistas. En el modelo de Bohr los electrones solo giraban en órbitas circulares. La excentricidad de la órbita dio lugar a un nuevo número cuántico: el número cuántico azimutal, que determina la forma de los orbitales, se lo representa con la letra l y toma valores que van desde 0 hasta n-1. Las órbitas son:
l = 0 se denominarían posteriormente orbitales s o sharp
l = 1 se denominarían p o principal.
l = 2 se denominarían d o diffuse.
l = 3 se denominarían f o fundamental.
Para hacer coincidir las frecuencias calculadas con las experimentales, Sommerfeld postuló que el núcleo del átomo no permanece inmóvil, sino que tanto el núcleo como el electrón se mueven alrededor del centro de masas del sistema, que estará situado muy próximo al núcleo al tener este una masa varios miles de veces superior a la masa del electrón.
Para explicar el desdoblamiento de las líneas espectrales, observado al emplear espectroscopios de mejor calidad, Sommerfeld supuso que las órbitas del electrón pueden ser circulares y elípticas. Introdujo el número cuántico secundario o azimutal, en la actualidad llamado l, que tiene los valores 0, 1, 2,…(n-1), e indica el momento angular del electrón en la órbita en unidades de h/2π , determinando los subniveles de energía en cada nivel cuántico y la excentricidad de la órbita.
Modelo atómico de Schrödinger
1926
% complete
El modelo atómico de Schrödinger concebía originalmente los electrones como ondas de materia. Así la ecuación se interpretaba como la ecuación ondulatoria que describía la evolución en el tiempo y el espacio de dicha onda material. Más tarde Max Born propuso una interpretación probabilística de la función de onda de los electrones. Esa nueva interpretación es compatible con los electrones concebidos como partículas cuasipuntuales cuya probabilidad de presencia en una determinada región viene dada por la integral del cuadrado de la función de onda en una región. Es decir, en la interpretación posterior del modelo, este era modelo probabilista que permitía hacer predicciones empíricas, pero en el que la posición y la cantidad de movimiento no pueden conocerse simultáneamente, por el principio de incertidumbre. Así mismo el resultado de ciertas mediciones no están determinadas por el modelo, sino solo el conjunto de resultados posibles y su distribución de probabilidad.
